安斯泰来CLDN18.2单抗申报上市| 晚期胃或胃食管交界处腺癌
2023年6月9日,安斯泰来宣布已向日本厚生劳动省提交了CLDN18.2单抗zolbetuximab的新药申请,用于一线治疗CLDN18.2阳性、HER2阴性的局部晚期不可切除或转移性胃或胃食管交界处腺癌。zolbetuximab将成为全球首个获批的CLDN18.2靶向治疗药物。

此次NDA是基于III期SPOTLIGHT和GLOW临床试验的结果:
Claudin 18.2单抗zolbetuximab联合CAPOX的III期临床研究(GLOW研究)
Claudin 18.2单抗zolbetuximab联合mFOLFOX6(Spotlight研究)的III期临床研究(Spotlight研究)
GLOW和SPOTLIGHT研究是安斯泰来胃癌药物开发计划的关键组成部分,该计划针对局部晚期不可切除或转移性胃癌或胃食管交界处腺癌患者的治疗需求开展研究,研究开发包括zolbetuximab在内的靶向治疗方案。
在这两项临床试验中,根据经验证的免疫组化检测分析,约38%的胃癌和胃食管交界癌患者符合CLDN18.2表达的阳性标准,即≥75%的肿瘤细胞中显示中至强染色强度的CLDN18.2。具体来看下目前公布的两项研究的一些数据。
GLOW研究
GLOW是一项全球、多中心、双盲、随机的III期试验,旨在评估zolbetuximab(IMAB362)+CAPOX(一种包括卡培他滨和奥沙利铂的联合化疗方案)与安慰剂+CAPOX一线治疗CLDN18.2阳性、HER2阴性的局部晚期不可切除或转移性胃癌或胃食管交界处腺癌患者的有效性和安全性。该研究覆盖166个研究中心,在美国、加拿大、英国、欧洲和亚洲招募了507名患者。主要终点是zolbetuximab联合CAPOX治疗对比安慰剂联合CAPOX治疗的无进展生存期。次要终点包括总生存期、客观缓解率、缓解持续时间、安全性和耐受性以及生活质量参数。
GLOW临床研究中,与安慰剂联合CAPOX组相比,zolbetuximab与CAPOX的联合用药组在无进展生存期(PFS)方面实现了统计学意义的显著提升。具体而言,相比于安慰剂联合CAPOX组,zolbetuximab与CAPOX联合用药将疾病进展或死亡风险降低了31.3%(n=507;风险比[HR]=0.687;[95%置信区间[CI]:(0.544-0.866)];P值=0.0007),达到GLOW研究的主要终点。治疗组和安慰剂组的中位无进展生存期分别为8.21个月(95%CI:7.46–8.84)和6.80个月(95%CI:6.14–8.08)。
该研究还显示在关键次要终点方面,zolbetuximab与CAPOX联合用药显著延长了总生存期(OS),将死亡风险降低了22.9%(风险比=0.771;95%CI:0.615-0.965;P值=0.0118)。治疗组和安慰剂组的中位总生存期分别为14.39个月(95%CI:12.29-16.49)和12.16个月(95%CI:10.28-13.67)。
研究中关于治疗期间严重不良事件(TEAE)方面,两组的发生率相近(zolbetuximab治疗组与安慰剂组分别为47.2%对49.8%)。在GLOW研究期间,zolbetuximab治疗组与安慰剂组最常见的治疗期间严重不良事件分别是恶心(68.5%对50.2%)、呕吐(66.1%对30.9%)和食欲下降(41.3%对33.7%)。
Spotlight研究
2023年1月20日,安斯泰来宣布将在2023 ASCO GI 大会上公布Claudin 18.2单抗zolbetuximab的III期研究Spotlight详细数据。
早在2022年11月17日,安斯泰来就宣布Claudin18.2抗体Zolbetuximab+化疗联合治疗Claudin18.2阳性、HER2阴性的复发性转移性胃癌的三期临床SPOTLIGHT达到主要终点。
Spotlight研究丨ASCO GI 23详细数据
研究要点:
Zolbetuximab是一种研究性单克隆抗体,其靶向CLDN18.2,一种在癌性胃上皮细胞上表达的蛋白质。
Claudin 18.2阳性、HER2阴性、局部晚期不可切除或转移性胃或GEJ患者随机1:1分配两组,分别采用Zolbetuximab加mFOLFOX6或安慰剂加mFOLFOX6的治疗方案。
Zolbetuximab联合mFOLFOX6治疗显著改善了无进展生存率和总生存率。
在Claudin 18.2(CLDN18.2)阳性、HER2阴性、局部晚期不可切除或转移性胃或胃食管接合部(GEJ)腺癌(LBA292)患者中,Zolbetuximab联合亚叶酸、氟尿嘧啶和奥沙利铂(mFOLFOX6)的一线治疗显著延长了无进展和总生存期。
研究原理和设计
Zolbetuximab是一种研究性单克隆抗体,其靶向CLDN18.2,一种在癌性胃上皮细胞上表达的蛋白质。早期的一项2期研究表明,Zolbetuximab联合化疗可提高局部晚期不可切除或转移性胃/GEJ腺癌患者的生存率。
在SPOTLIGHT试验中,参与者被随机分配为1:1服用Zolbetuximab加mFOLFOX6(283名参与者)或安慰剂加mFORFOX6,282名参与者)。主要终点是无进展生存率(根据RECIST 1.1,独立审查委员会)。总生存率是次要终点,仅在无进展生存率具有统计学意义时计算。
参与者的中位年龄为62岁,62%为男性,69%为非亚裔,31%为亚裔。77%的参与者的主要部位是胃,22.6%的参与者在≥3个器官中有转移。
研究结果
疗效结果汇总在表中。Zolbetuximab联合mFOLFOX6治疗显著改善了无进展生存率和总生存率,这一发现在大多数分析的亚组中是一致的。
Shitara博士说:“这显然是一项积极的试验,有望获得Zolbetuximab的监管批准,尤其是对于CLDN18.2阳性的患者,将成为标准治疗,尤其是对于CLDN18.2阳性的患者。”他还指出,在这一患者群体中进行的全球试验中,观察到的18个月总生存期中位数是罕见的。
在Zolbetuximab加mFOLFOX6组中,最常报告的治疗紧急不良事件是恶心(81.0%vs 60.8%,在唑贝妥昔单抗组vs安慰剂组)、呕吐(64.5%vs 34.5%)和食欲下降(47.0%vs 33.5%)。
两个治疗组的严重不良事件发生率相似(44.8%Zolbetuximab+mFOLFOS6 vs 43.5%安慰剂+mFORFOX6)。
“Zolbetuximab是自十多年前曲妥珠单抗(trastuzumab)以来,除免疫检查点抑制剂外的第一种分子靶向治疗,在晚期胃癌和GEJ癌症的一线治疗中显示出具有统计学意义的生存益处。”——David H.Wang博士
Claudin 18.2 靶点研发加速内卷
2022年10月1日,信达生物IBI343的临床试验申请获得NMPA受理。IBI343是信达生物内研首款ADC,靶点为claudin18.2,具有旁观者效应,能够杀伤抗原低表达癌细胞。由此可见,信达生物也开始布局已经有内卷趋势的claudin18.2靶点,且是以ADC的药物形式。
2022年12月8日,荣昌生物宣布:公司注射用RC118获得美国食品药品监督管理局(FDA)颁发的两项孤儿药资格认定,分别针对胃癌(包括胃食管交界癌)和胰腺癌适应症。注射用RC118是荣昌生物自主研发的创新型抗体偶联药物(ADC),用于治疗Claudin 18.2表达阳性的局部晚期不可切除或转移性恶性实体瘤患者。该产品于2021年9月获得国家药品监督管理局药品审评中心(CDE)的I期临床试验批件。目前,正在进行剂量爬坡研究,并表现出良好的安全性与耐受性。
2022年3月11日,据CDE官网公示,共有三款CLDN18.2靶向药物临床试验申请获批,分别为:
再鼎医药CLDN18.2单抗ZL-1211;
君实生物的CLDN18.2 ADC JS107,也是君实生物进入临床阶段的第2款靶向CLDN18.2的药物。另一款CLDN18.2单抗JS012已于2021年11月获批临床;
普米斯生物Claudin18.2/4-1BB双抗-PM1032 注射液。
上述的企业都在布局基于Claudin18.2的单抗或ADC药物,而普米斯开始尝试基于Claudin18.2为基础靶点,进行双抗的研究探索(Claudin18.2/4-1BB双抗)。
Claudin 蛋白结构
在介绍Claudin 18.2(CLDN 18.2)靶点前,首先得介绍Claudins,Claudins是一类存在于上皮和内皮紧密连接中的整合素膜蛋白,最早由Shoichiro Tsukita等于1998年发现。Claudins蛋白家族共有24个成员,具有4个跨膜结构域。其中,NH2端和COOH端位于胞内,具有两个胞外环。这种结构使得Claudins紧密蛋白家族能够有效维持上皮细胞和内皮细胞的极性,从而有效调控细胞旁通透性和电导。
有研究表明,Claudin蛋白表达的改变会导致紧密连接功能受损,影响信号传导途径,并在某些上皮癌中起到促肿瘤作用。正常组织由于细胞间紧密粘连, 抗体药物极难与其结合。然而, 癌细胞组织间隙的松散结构却使CLDN18.2暴露于蛋白类大分子药物下变成可能, 因此CLDN18.2是一个理想的新一代抗肿瘤治疗靶点。此外,不同的Claudin蛋白在正常组织中的表达谱也有差异。以胃癌为例,Claudin 18.2特异地表达在分化的胃黏膜上皮细胞,但在胃干细胞区不表达。虽然基于HER2的胃癌靶向药物已获批多款,但胃癌患者的HER2阳性突变率很低,大约只有10%~20%。而Claudin 18.2在所有胃癌患者中的阳性率可以达到近60%,具有更广泛的患者获益可能。所以,Claudin 18.2靶点竞争激烈,是有原因的。
2021年7月8日,专注于自免及肿瘤疾病领域的Biotech企业—康诺亚生物,正式在港交所上市。研发管线中的CMG901,为为全球首个Claudin 18.2 ADC药物,由康诺亚与乐普生物旗下美雅珂联合研发。
小鼠胃癌PDX模型研究中,CMG901表现出远远优于Claudin 18.2抗体的抗肿瘤活性。
下表汇总了目前为止Claudin 18.2在研项目信息:
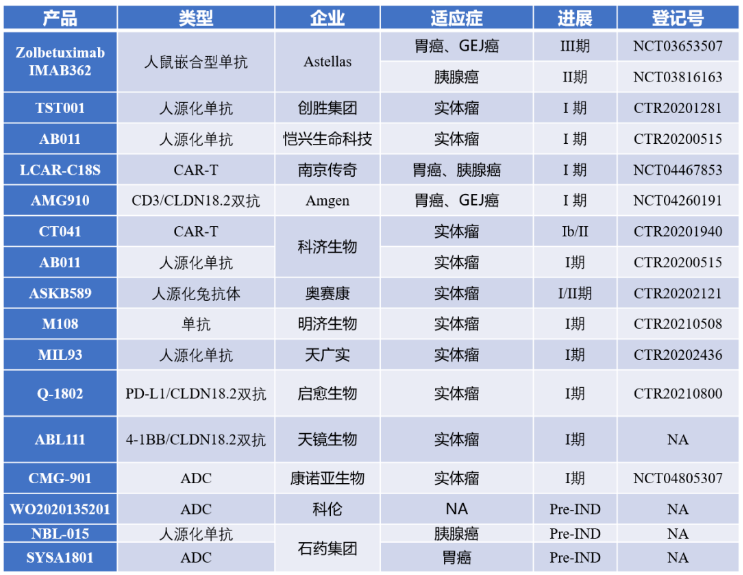
资料来源:ClinicalTrials,CDE,各公司官网
总结
Her2在胃癌领域的成功探索,极大地促进了ADC药物的研发进展,相较于Trop2 ADC项目的接连失败,基于已成药靶点的探索,是价值回调后的稳妥选择。而胃癌患者的低Her2阳性率,让很多胃癌患者无缘Her2靶向药物,亟待新靶点新药物的惠及。Claudin 18.2靶点的高阳性率及目前的临床在研数据披露,令人振奋。 期望能够在如此众多的产品类型中,成功实现商业化,惠及更多的患者。
来源 | 健康界
版权归原作者所有,若有违规、侵权请联系我们

- 1


